“환자에 미칠 위험성 낮아”…경찰, 전현직 임직원 등 수사 중

[서울이코노미뉴스 김준희 기자] 식품의약품안전처는 13일 코스닥 상장 의료기기 업체인 한스바이오메드가 실리콘겔 인공유방 ‘벨라젤’을 허가사항과 다른 원료를 사용해 제조·유통한 사실을 확인했다고 밝혔다.
실리콘겔 인공유방은 유방을 재건하거나 성형하는데 사용되는 제품이다.
식약처에 따르면 한스바이오메드는 2015년 12월부터 허가사항과 다른 원료를 사용해 부적합한 인공유방을 생산해 7만여개를 의료기관에 공급했다.
한스바이오메드는 전 제조업무정지 6개월의 행정처분을 받는다.
수사 결과에 따라서는 5년 이하의 징역 또는 5000만원 이하의 벌금을 물 수 있다.
이와 관련, 경기남부지방경찰청 지능범죄수사대는 한스바이오메드의 불법 행위와 관련해 전현직 임직원들을 대상으로 수사를 진행 중이다.
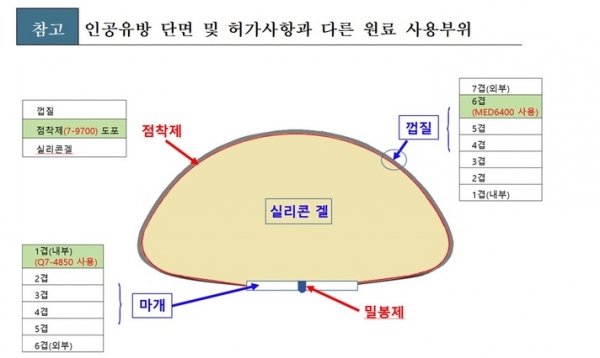
한스바이오메드가 사용한 문제의 원료는 총 5종이다.
이 가운데 실리콘 접착제는 피부접촉 의료기기(상처보호제)에, 나머지 4종은 국내 허가된 다른 인체이식 의료기기(인공유방, 심장판막 등)에 사용되는 원료다.
식약처는 해당 인공유방 품목에 대한 판매중지 및 회수를 명령하고, 성형학회, 의사협회 등 관련 단체를 통해 의료기관에 해당 제품 사용을 중지토록 요청했다.
문제의 원료는 미국 다우코닝이 제작한 실리콘 접착제인 ‘7-9700’와 탄성을 지닌 실리콘 원료인 ‘Q7-4850’이다. 이들 원료는 주로 인체 외부에 부착하는 반창고 등을 제조할 때 사용하고 있다.
한스바이오메드는 인공유방의 쉘과 실리콘겔 사이를 붙이는데 ‘7-9700’를, 쉘을 밀봉하는 마개 재료로 ‘Q7-4850’를 사용했다.
‘7-9700’과 ‘Q7-4850’은 모두 고온에서 1급 발암물질인 포름알데히드를 배출한다. 한스바이오메드의 벨라젤은 제조 과정에서 섭씨 150~160도에 이르는 열처리 공정을 4~8시간 거치는 것으로 전해졌다.
식약처는 그러나 전문가 자문회의를 통해 이 원료를 사용한 인공유방이 이식환자에 미칠 위험성은 낮다고 판단했다.
정상적 상태에서 인공유방 밖으로 누출될 가능성이 매우 적다는 것이다. 그리고 고온에서 발생 가능성이 있는 포름알데히드도 이후 내부 공기제거 과정을 거치기 때문에 제품에 잔류할 가능성이 적다는 것이 전문가의 견해였다는 게 식약처의 설명이다.
식약처는 현재 건강보험심사평가원을 통해 해당 제품을 이용해 유방재건술을 받은 환자 현황을 파악 중이다.
한스바이오메드에는 이식환자에 대한 보상방안을 마련해 제출하도록 조치했다. 진단·검사비, 부작용 시 보상대상·범위·기간을 조속히 확정할 계획이다.